Fortschritt für die Knochen-Forschung
Hochauflösendes Verfahren zur Nano-Computertomographie entwickelt
2010-09-30 – Nachrichten aus dem Physik-Department
Ein neuartiges Nano-Tomographieverfahren, das von einem Team aus Forschern der Technischen Universität München (TUM), des Paul Scherrer Instituts (PSI) und der ETH Zürich entwickelt wurde, erlaubt erstmals computertomographische Untersuchungen feinster Strukturen mit einer Auflösung im Nanometerbereich. Mit Hilfe der neuen Methode können etwa dreidimensionale Innenansichten fragiler Knochenstrukturen erstellt werden. Die ersten mit diesem Verfahren erzielten Nano-CT-Bilder werden am 23. September 2010 in der renommierten Fachzeitschrift Nature veröffentlicht. Die neue Technik kann Lebens- und Materialwissenschaften gleichermaßen voranbringen.

Franz Pfeiffer vor dem von ihm und seinem Team entwickelten Experimentieraufbau an der Synchrotron Lichtquelle Schweiz des Paul Scherrer Instituts, an dem das neue Nanotomographieverfahren entwickelt wurde. © TU München
Osteoporose, auch Knochenschwund genannt, ist eine der häufigsten Erkrankungen des alternden Knochens: In Deutschland ist etwa ein Viertel der Bevölkerung über 50 Jahre davon betroffen. Bei den Patienten schrumpft die Knochensubstanz übermäßig rasch, damit steigt das Risiko für Brüche deutlich. In der klinischen Forschung wird Osteoporose bisher fast ausschließlich über die Messung einer allgemein verringerten Knochendichte bestimmt. Diese sagt jedoch wenig über die damit verbundenen und ebenso wichtigen lokalen Struktur- und Knochendichte-Änderungen aus. Franz Pfeiffer, TUM-Professor für Biomedizinische Physik und Leiter des Forscherteams, hat das Dilemma gelöst: „Mit unserem neu entwickelten Nano-CT-Verfahren ist es jetzt möglich, die Struktur- und Dichte-Änderungen des Knochens hochaufgelöst und in 3D darzustellen. Damit kann man die der Osteoporose zugrunde liegenden Strukturänderungen auf der Nanoskala erforschen und bessere Therapieansätze entwickeln.“
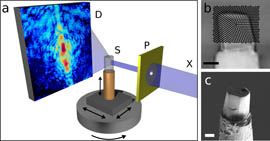
Schematische Darstellung des neuen Nano-CT-Verfahrens. © TU München
Pfeiffers Team hat bei der Entwicklung auf der Röntgen-Computertomographie (CT) aufgebaut. Ihr Prinzip ist seit langem bekannt – CT-Geräte werden im Krankenhaus und in der Arztpraxis tagtäglich zur diagnostischen Durchleuchtung des menschlichen Körpers verwendet. Hierbei wird der Körper mit Röntgenstrahlen durchleuchtet. Ein Detektor misst dabei unter verschiedenen Winkeln, wie viel Röntgenstrahlung jeweils absorbiert wird. Im Prinzip werden einfach Röntgenbilder aus verschiedenen Richtungen aufgenommen. Aus einer Vielzahl solcher Aufnahmen können dann mittels Bildverarbeitung digitale 3D-Bilder des Körperinneren erzeugt werden.
Die neu entwickelte Methode misst nun für jeden Beleuchtungswinkel nicht nur die gesamte vom untersuchten Objekt absorbierte Intensität, sondern auch die Teile des Röntgenstrahls, die in verschiedene Richtungen abgelenkt – in Physikersprache „gestreut“ – werden. Diese erzeugen für jeden Punkt ein Streubild, das zusätzliche Informationen über die genaue Nanostruktur liefert, da die Röntgenstreuung gerade auf allerkleinste Strukturänderungen sensitiv ist. „Da wir dabei sehr viele Einzelbilder extrem präzise aufnehmen und verarbeiten müssen, war bei der Implementierung des neuen Verfahrens die Verwendung hochbrillanter Röntgenstrahlung und schneller, rauscharmer Pixel-Detektoren besonders wichtig – beides steht an der Synchrotron Lichtquelle Schweiz (SLS) zur Verfügung“, so Oliver Bunk, der an der vom schweizerischen PSI betriebenen Synchrotronlichtquelle den entsprechenden Experimentierplatz mit aufgebaut hat.
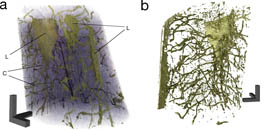
Aus vielen Röntgenstreubildern (links angedeutet) berechnet der speziell entwickelte Nano-CT-Algorithmus ein hochaufgelöstes dreidimensionales digitales Bild der Probe. © TU München
Die Streubilder werden anschließend mit einem Algorithmus verarbeitet, der von dem Team entwickelt wurde. TUM-Forscher Martin Dierolf, Erstautor des Nature-Artikels, erklärt: „Wir haben einen Bildrekonstruktionsalgorithmus entwickelt, der aus den über hunderttausend Streubildern ein hochaufgelöstes dreidimensionales Bild der Probe errechnet. Dabei berücksichtigt der Algorithmus nicht nur die klassische Röntgenabsorption, sondern die wesentlich sensitivere Beeinflussung der Phase der Röntgenwellen.“ Exemplarisch wurde mit der neuen Technik die mit 25 Mikrometern härchenfeine Knochenprobe einer Labormaus untersucht – mit überraschend exakten Ergebnissen. Die so genannten Phasenkontrast-CT-Aufnahmen stellen selbst kleinste Dichteunterschiede in der Knochenprobe extrem genau dar: Querschnitte durch Hohlräume, in denen Knochenzellen eingebettet sind, und deren rund 100 Nanometer feines Verbindungsnetzwerk sind gut erkennbar.
„Das neue Nano-CT-Verfahren erreicht zwar nicht die Ortsauflösung, die derzeit in der Elektronenmikroskopie möglich ist, kann aber – aufgrund des hohen Durchdringungsvermögens von Röntgenstrahlung – dreidimensionale Tomographiebilder von Knochenproben liefern“ kommentiert Roger Wepf, Leiter des Elektronenmikroskopiezentrums (EMEZ) an der ETH Zürich. „Darüber hinaus zeichnet sich das neue Nano-CT-Verfahren durch seine hohe Genauigkeit in der Knochendichtebestimmung aus, welche gerade für die Knochenforschung von entscheidender Bedeutung ist.“ Mithilfe des Verfahrens wird man insbesondere die Frühphase der Osteoporose-Erkrankung genauer studieren sowie Behandlungserfolge verschiedener Therapien in klinischen Studien evaluieren können.
Aber die neue Technik ist auch außerhalb der Medizin sehr nützlich: Weitere Anwendungsfelder liegen in der Entwicklung neuer Werkstoffe in den Materialwissenschaften oder in der Charakterisierung von Halbleiterbauelementen. Schließlich lässt sich das Nano-CT-Verfahren auch auf neuartige, laser-basierte Röntgenquellen übertragen, so wie sie derzeit im Rahmen des Exzellenzclusters „Munich-Centre for Advanced Photonics“ (MAP) und am neu bewilligten Großforschungsprojekt „Centre for Advanced Laser Applications“ (CALA) auf dem TUM-Campus Garching bei München entwickelt werden.
Weitere Informationen
Originalpublikation
Ptychographic X-Ray Computed Tomography at the Nano-Scale
Martin Dierolf, Andreas Menzel, Pierre Thibault, Philipp Schneider, Cameron M. Kewish, Roger Wepf, Oliver Bunk, Franz Pfeiffer
Nature, 23. September 2010 – DOI: 10.1038/nature09419
Bildmaterial zum Download
http://mediatum.ub.tum.de/?cunfold=997485&dir=997485&id=997485
Animation
http://users.physik.tu-muenchen.de/gu45ten/franz_pfeiffer/bone_nanoCT.mov
Die Animation zeigt die erste Nano-CT Aufnahme einer Knochenprobe mit einem Durchmesser von ca. 25 Mikrometer. Deutlich zu sehen sind die feinen, ca. 100 Nanometer großen Verästelungen (Kanalikuli), die das Verbindungsnetzwerk zwischen den Knochenzellen (Osteocyten) bilden.
Kontakt
Prof. Dr. Franz Pfeiffer
Lehrstuhl für Biomedizinische Physik
Technische Universität München
James-Franck-Straße 1
85748 Garching, Germany
Tel.: +49 89 289 12551
Fax: +49 89 289 12548
E-Mail: nelly.de.leiris@mytum.de
Internet: http://www.physik.tu-muenchen.de/lehrstuehle/E17/
Dr. Oliver Bunk
Labor für Makromoleküle und Bioimaging
Paul Scherrer Institut
5232 Villigen PSI, Schweiz
Tel.: +41 56 310 3077
E-Mail: oliver.bunk@psi.ch
Internet: http://www.psi.ch
Dr. Roger Albert Wepf
EMEZ – Electronen Microscopy ETH Zürich
ETH Zürich
Wolfgang-Pauli-Str. 16
8093 Zürich, Schweiz
Tel: +41 44 633 45 58
E-Mail: roger.wepf@emez.ethz.ch
Internet: www.ethz.ch